1. Основные характеристики хлорита натрия
2. Использование хлорита натрия в очистке воды
3. Сравнительный анализ эффективности
4. Дозировки, методы применения и контроль параметров
- Оптимальные концентрации для различных типов воды.
- Влияние на pH, жесткость и другие параметры.
- Совместимость с другими реагентами.
- Дополнительно: Таблица совместимости хлорита натрия с различными химическими веществами.
5. Практические аспекты и бизнес-решения
- Где и как выгодно применять хлорит натрия?
- Оборудование и технологии дозирования.
- Оптимизация затрат на реагенты.
- Дополнительно: Пример расчета расхода реагента для конкретного случая.
Основные характеристики хлорита натрия
Химическая формула, структура и свойства

Хлорит натрия (NaClO₂) — это неорганическое соединение, представляющее собой соль натрия и хлористой кислоты. В чистом виде он образует бесцветные кристаллы, хорошо растворимые в воде и этаноле.
Основные физико-химические параметры:
- Химическая формула: NaClO₂
- Молярная масса: 90,44 г/моль
- Плотность: 2,468 г/см³
- Растворимость: 60 г/100 мл воды при 20°C
- Кристаллогидрат: NaClO₂·3H₂O
При нагревании или контакте с кислотами хлорит натрия разлагается с выделением активного хлора и кислорода. В нейтральной или слабощелочной среде он стабилен, что делает его удобным для хранения и транспортировки.
Окислительные свойства и их значение в водоочистке
Хлорит натрия проявляет высокую окислительную активность, особенно в кислых растворах. Под воздействием кислот он разлагается с образованием диоксида хлора (ClO₂), который используется как эффективное дезинфицирующее средство.
Ключевые окислительные реакции хлорита натрия в водных растворах:
- Окисление железа и марганца (удаление Fe²⁺ и Mn²⁺ из воды):
2Fe(HCO3)2+NaClO2+H2O→2Fe(OH)3↓+4CO2↑+NaCl
(В результате образуется осадок гидроксида железа, который легко удаляется фильтрацией.)
- Разложение хлорита натрия в кислой среде:
2NaClO2→2NaCl+Cl2+O2
(Выделяется газообразный хлор, который способствует дезинфекции воды.)
Благодаря этим реакциям хлорит натрия активно используется в системах водоподготовки. Он эффективно устраняет растворенные металлы, снижает содержание органических примесей и обеспечивает дезинфекцию воды без образования канцерогенных побочных продуктов, что делает его безопасной альтернативой традиционному хлорированию.
Взаимодействие с органическими загрязнителями и патогенами
При контакте с органическими веществами и микроорганизмами хлорит натрия демонстрирует мощное антимикробное действие.
Механизм дезинфекции:
- Окисление клеточных белков и разрушение мембран бактерий.
- Дестабилизация оболочек вирусов.
- Разрушение спор грибков, что предотвращает их дальнейшее размножение.
Использование хлорита натрия эффективно против Legionella, Escherichia coli, Salmonella и других опасных микроорганизмов. В отличие от традиционного хлорирования, он не приводит к образованию тригалометанов, что делает его безопасным и эффективным средством для водоподготовки.
Использование хлорита натрия в очистке воды
Хлорит натрия активно применяется в очистке сточных и питьевых вод, обеспечивая удаление органических и неорганических загрязнителей, уничтожение патогенных микроорганизмов и предотвращение образования токсичных побочных соединений.
Промышленные сточные воды: удаление металлов, нефтепродуктов и токсичных соединений
В промышленности хлорит натрия используется для очистки сточных вод предприятий металлургии, химической, нефтеперерабатывающей и пищевой промышленности. Его эффективность обусловлена сильными окислительными свойствами, которые позволяют разлагать опасные вещества.
Как хлорит натрия удаляет промышленные загрязнители?
| Загрязнитель | Механизм удаления | Оптимальный pH |
| Тяжелые металлы (Fe²⁺, Cu²⁺, Pb²⁺, Zn²⁺) | Окисление до нерастворимых гидроксидов с последующим осаждением | 6,5–8,5 |
| Нефтепродукты | Разложение углеводородов путем окисления | 5,5–7,5 |
| Цианиды (CN⁻) | Окисление до нетоксичных соединений | 8–9 |
| Фенолы | Окисление до углекислого газа и воды | 6–7 |
Таким образом, правильный подбор дозировки хлорита натрия и контроль pH позволяют значительно снизить концентрацию опасных веществ и обеспечить их удаление.
Городские очистные сооружения: обработка биологических загрязнителей

В городских системах водоотведения хлорит натрия применяется для обеззараживания сточных вод перед их сбросом или повторным использованием.
Какие микроорганизмы эффективно уничтожает хлорит натрия?
- Бактерии (Escherichia coli, Salmonella, Legionella).
- Вирусы (включая гепатит А и ротавирусы).
- Простейшие паразиты (Cryptosporidium, Giardia).
Одним из ключевых преимуществ хлорита натрия является его способность окислять биологические загрязнители без образования тригалометанов (ТГМ), которые могут образовываться при традиционном хлорировании.
Влияние pH на эффективность обеззараживания
(График показывает, как изменяется скорость уничтожения бактерий и вирусов в зависимости от pH раствора.)
Исследования показывают, что наибольшая эффективность обеззараживания достигается при pH 5,5–7,5, так как в этом диапазоне диоксид хлора образуется в максимальных количествах.
Питьевая вода: механизмы обеззараживания и особенности применения
Хлорит натрия используется для дезинфекции и улучшения качества питьевой воды, заменяя традиционные методы обработки.
Как он работает?
- Образует диоксид хлора (ClO₂), который уничтожает бактерии, вирусы и грибки.
- Окисляет органические примеси, снижая уровень гуминовых кислот, влияющих на цвет и запах воды.
- Удаляет железо и марганец путем перевода их в нерастворимые формы.
Таблица: Эффективность хлорита натрия в питьевой воде
| Загрязнитель | Результат обработки | Время реакции |
| Железо (Fe²⁺) и марганец (Mn²⁺) | Осаждение в виде гидроксидов | 10–30 мин |
| Гуминовые кислоты (цвет, мутность) | Окисление до простых соединений | 15–45 мин |
| Бактерии и вирусы | Полное уничтожение | 5–20 мин |
(График зависимости скорости удаления органических и биологических загрязнителей от концентрации хлорита натрия.)
Благодаря высокой скорости реакции и отсутствию токсичных побочных продуктов, хлорит натрия является надежным и безопасным средством водоочистки, широко применяемым на муниципальных водоочистных станциях и в частных системах водоподготовки.
Сравнительный анализ эффективности хлорита натрия в водоочистке
При выборе метода обработки воды важно учитывать способность уничтожать микроорганизмы, влияние на качество воды, а также остаточные вещества и стоимость обработки. Хлорит натрия является одним из самых сбалансированных реагентов, обеспечивающим высокую степень очистки при оптимальных затратах.
| Параметры | Хлорит натрия (NaClO₂) | Гипохлорит натрия (NaOCl) | Озонирование | Хлорирование |
| Эффективность против микроорганизмов | Высокая | Очень высокая | Очень высокая | Высокая |
| Эффективность против химических загрязнителей | Высокая | Умеренная | Высокая | Низкая |
| Остаточные вещества | Низкие | Средние | Отсутствуют | Высокие |
| Влияние на качество воды | Минимальное | Может вызывать привкус | Улучшает качество | Может вызывать привкус |
| Стоимость обработки 1 м³ воды | Средняя | Низкая | Высокая | Низкая |
Эффективность против микроорганизмов и химических загрязнителей
Хлорит натрия и озонирование обладают высокой эффективностью против вирусов, бактерий и простейших, а также способны разрушать органические загрязнители, включая фенолы, гуминовые кислоты и нефтепродукты.
- Гипохлорит натрия хорошо борется с микроорганизмами, но его эффективность снижается при высоких значениях pH.
- Хлорирование менее эффективно против химических соединений, но стабильно работает для обеззараживания.
Использование хлорита натрия позволяет достичь сбалансированной эффективности, обеспечивая биологическую и химическую очистку воды.
Остаточные вещества и их влияние на качество воды
Методы водоочистки отличаются по количеству остаточных соединений, которые могут влиять на вкус, запах и безопасность воды.
- Хлорит натрия оставляет минимальное количество побочных продуктов, что делает его безопасным для питьевой воды.
- Гипохлорит натрия может образовывать тригалометаны (ТГМ), влияющие на вкус и запах воды.
- Озонирование не оставляет остаточных веществ, улучшая кислородный баланс воды.
- Хлорирование формирует наибольшее количество остаточных соединений, что может повлиять на безопасность питьевой воды.
Благодаря низкому уровню остаточных соединений, хлорит натрия подходит для обработки питьевой воды, обеспечивая стабильный химический состав.
Стоимость обработки 1 м³ воды разными методами
При выборе реагента важно учитывать экономическую целесообразность.
- Хлорирование и гипохлорит натрия – самые доступные методы, но они требуют дополнительных затрат на устранение побочных продуктов.
- Хлорит натрия – имеет среднюю стоимость, но обеспечивает стабильное качество без образования токсичных соединений.
- Озонирование – самый дорогой метод из-за затрат на оборудование и высокое энергопотребление.
График зависимости эффективности очистки от дозировки реагента
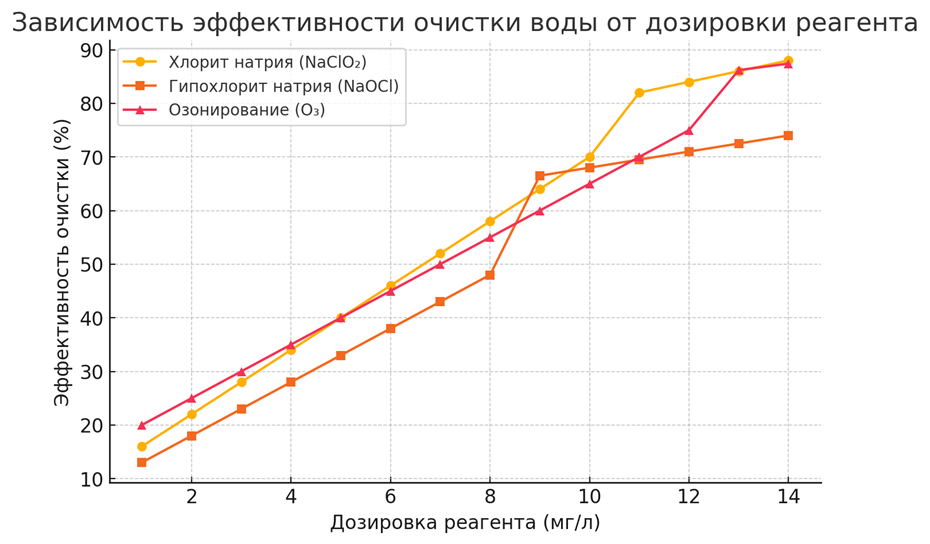
(График демонстрирует, как изменяется эффективность дезинфекции воды при увеличении дозировки хлорита натрия, гипохлорита натрия и озонирования.)
Анализ показывает:
- Эффективность очистки хлоритом натрия возрастает при дозировке 5–10 мг/л, после чего дальнейшее повышение концентрации не дает значительного прироста.
- Гипохлорит натрия менее эффективен при высоких значениях pH, что требует дополнительной корректировки состава воды.
- Озонирование стабильно эффективно, но требует точного контроля концентрации и времени обработки.
Использование оптимальной дозировки реагента позволяет повысить эффективность очистки воды, снизить расход химикатов и минимизировать образование побочных продуктов.
Хлорит натрия – это сбалансированное решение для водоочистки, которое сочетает высокую эффективность, безопасность и экономичность.
- Безопаснее хлорирования – меньше побочных соединений.
- Эффективнее гипохлорита натрия – справляется с химическими загрязнителями.
- Доступнее озонирования – не требует сложного оборудования.
Выбор метода зависит от конкретных условий очистки, но хлорит натрия остается одним из самых перспективных реагентов для промышленных и муниципальных систем водоочистки.
Дозировки, методы применения и контроль параметров
Хлорит натрия активно используется в системах водоочистки благодаря своим сильным окислительным свойствам. Однако для достижения максимальной эффективности и безопасности важно учитывать оптимальные концентрации, влияние на параметры воды и совместимость с другими реагентами.
Оптимальные концентрации для различных типов воды
Выбор дозировки хлорита натрия зависит от степени загрязнения воды и конкретных задач обработки.
|
Тип воды |
Оптимальная дозировка (мг/л) |
|
Промышленные сточные воды |
10–50 (в зависимости от уровня загрязнения) |
|
Городские очистные сооружения |
5–20 (для дезинфекции и устранения биологических загрязнителей) |
|
Питьевая вода |
1–5 (для обеззараживания и улучшения качества) |
В промышленности хлорит натрия используется в высоких концентрациях из-за большого количества токсичных и органических загрязнителей. В то же время при обработке питьевой воды дозировка должна быть минимальной, чтобы обеспечить безопасность потребителей.
Влияние на pH, жесткость и другие параметры
Обработка воды хлоритом натрия не только уничтожает загрязнители, но и может оказывать влияние на химический баланс воды.
- pH воды: Хлорит натрия незначительно повышает уровень pH, но его влияние меньше, чем у гипохлорита натрия, который увеличивает щелочность воды. В отличие от традиционного хлорирования, он не приводит к снижению pH, что делает его более стабильным реагентом.
- Жесткость воды: Хлорит натрия не влияет на жесткость, поскольку не взаимодействует с кальцием и магнием. Это его преимущество перед некоторыми другими реагентами, которые могут изменять минеральный состав воды.
- Общая щелочность: Хлорит натрия может снижать щелочность воды, что важно учитывать при обработке питьевой воды и бассейнов. Контроль этого параметра позволяет избежать дисбаланса и предотвратить коррозию трубопроводов.
Таким образом, правильное дозирование хлорита натрия позволяет не только эффективно очищать воду, но и минимизировать влияние на её состав.
Совместимость с другими реагентами
Использование хлорита натрия в сочетании с другими химическими веществами может увеличить эффективность обработки. Однако важно учитывать возможные химические реакции, которые могут происходить при смешивании веществ.
| Химическое вещество | Совместимость |
| Гипохлорит натрия (NaClO) | Слабая |
| Хлорид натрия (NaCl) | Хорошая |
| Нитрат натрия (NaNO₃) | Хорошая |
| Карбонат натрия (Na₂CO₃) | Хорошая |
| Сульфат натрия (Na₂SO₄) | Хорошая |
| Хлористая кислота (HCl) | Очень хорошая |
Основные рекомендации по совместимости:
- Смешивание с кислотами (например, HCl) приводит к образованию диоксида хлора (ClO₂), который используется как мощный дезинфектант.
- Совместимость с неорганическими солями натрия позволяет использовать хлорит натрия в комбинированных схемах очистки воды.
- Гипохлорит натрия плохо сочетается с хлоритом натрия, так как их совместное применение может привести к нежелательным побочным реакциям.
График зависимости эффективности очистки от дозировки реагента
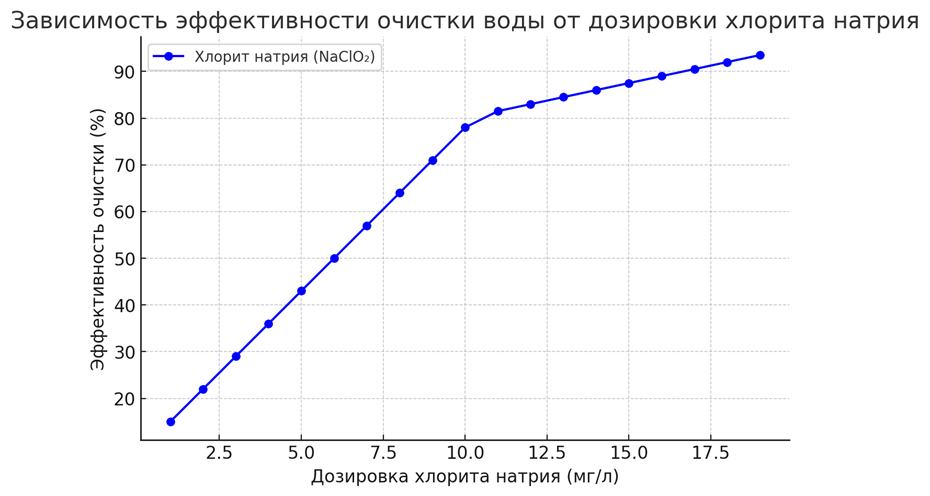
(График показывает, как увеличивается эффективность очистки воды при повышении дозировки хлорита натрия.)
Исследования показывают, что:
- При увеличении дозировки от 1 до 10 мг/л эффективность обработки растет линейно.
- При превышении 10 мг/л дальнейшее повышение дозировки не приводит к значительному улучшению очистки, но может вызывать образование побочных продуктов.
- Оптимальная концентрация хлорита натрия для питьевой воды составляет 5–10 мг/л, что обеспечивает максимальную дезинфекцию без негативного влияния на состав воды.
Правильное применение хлорита натрия требует учета его дозировки, влияния на параметры воды и совместимости с другими реагентами.
- Оптимальные дозировки зависят от типа воды: для промышленных стоков – до 50 мг/л, для питьевой – не более 5 мг/л.
- Влияние на pH и жесткость минимальное, что делает его удобным в применении.
- Сочетание с кислотами позволяет получить мощный дезинфектант, но необходимо избегать смешивания с гипохлоритом натрия.


